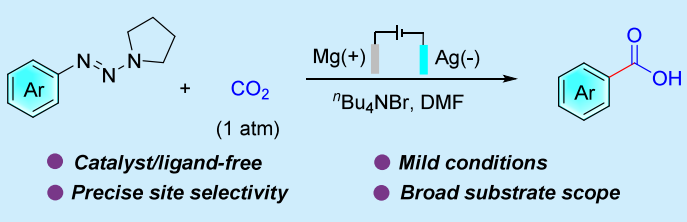
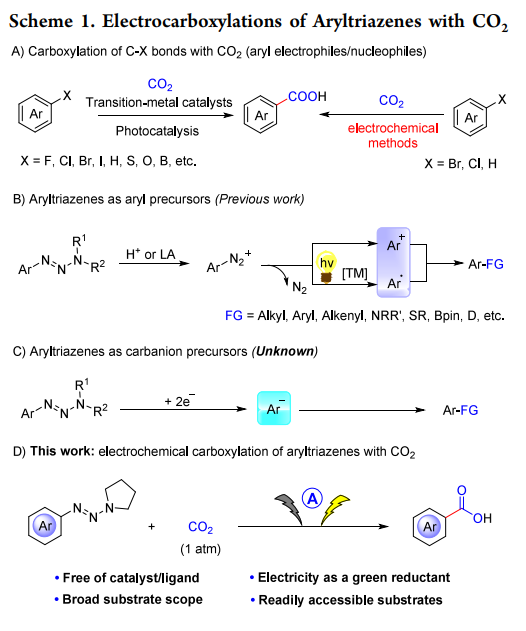
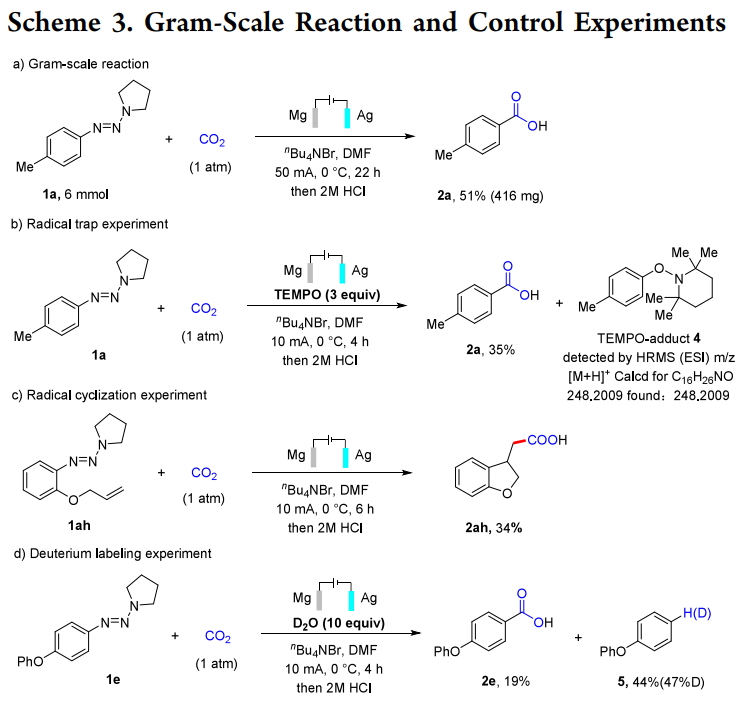
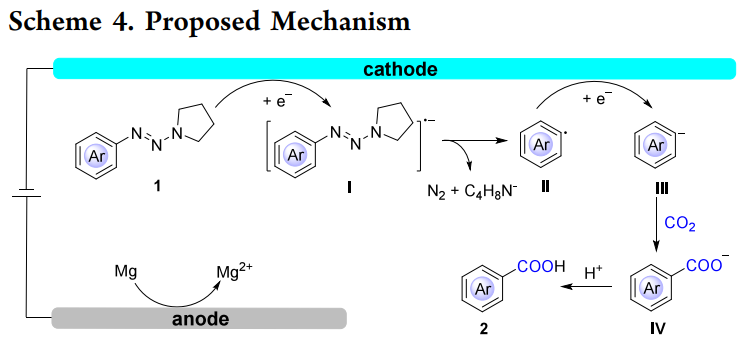
二氧化碳是一种来源丰富、无毒且可再生的C1合成子。从可持续发展的化学角度来看,通过化学转化将其应用于高附加值的能源分子、材料和化学品的合成具有重要意义。这不仅推动了可持续化学发展,还助力实现碳中和并减少对石油化工的依赖。芳基羧酸作为一种重要的骨架结构,在众多天然产物、药物及有机材料中作为核心结构单元存在。目前通过热催化和光催化二氧化碳C(sp2 )−X键的羧基化反应可合成芳基羧酸(Scheme 1A)。虽然在有机合成领域有很多可靠的合成方法,但大多数策略需要昂贵的过渡金属或化学计量的还原剂,这限制了它们在合成化学中的进一步应用。此外,C−N键的还原羧化反应很少被报道。因此,开发新合成技术以廉价原料来合成羧酸意义重大且面临挑战。有机电化学利用 “无痕” 的电子作为氧化还原试剂,是构建新化学键的高效且高选择性策略。电化学反应具有可连续调节和控制的电流电位,能轻松达到还原电位,调节产物选择性,进而促进芳基前体的还原。因此,芳烃及其衍生物的电化学羧化是生成芳基羧酸的一种有前景且有效的策略。直接的C−H键羧化在该领域具有潜力,但在底物适应和提高产物选择性方面仍需进一步研究 。最近,先后有报道称镍催化的有机卤化物电羧化反应及有机介质介导的电羧化反应,这体现了有机卤化物作为芳基前体在电羧化反应中的强大作用。为了扩大电羧化反应的适用范围,探索新的芳基前体仍至关重要。在各种芳香族衍生物中,芳基三氮烯可由芳胺轻松合成,具稳定性好、反应位点多及反应条件温和等优势。作为芳基重氮盐的稳定替代品,芳基三氮烯在构建 C(sp² )−C / 杂原子键以实现后期官能化方面被广泛应用。在反应中,芳基三氮烯通常会被酸活化生成芳基重氮阳离子,进而转化为芳基自由基或芳基阳离子并进行后续转化(Scheme 1B)。尽管该领域已取得显著进展,芳基三氮烯仍是相关芳基自由基和芳基阳离子的优质前体。据目前所知,尚未有通过电子还原从芳基三氮烯生成芳基阴离子的报道。此外,由于缺乏有效的还原体系,芳基三氮烯中 C(sp² )−N 键的电化学活化和官能化目前仍未被研究(Scheme 1C)。基于对二氧化碳羧基化反应的研究兴趣,作者提出芳基三氮烯或许能在阴极经双电子还原生成芳基阴离子,进而与二氧化碳发生羧基化反应。然而,副反应倾向(包括质子化、同系耦合和产物的脱羧反应)以及二氧化碳的惰性,给电化学还原条件下的顺利转化带来了挑战。基于此,南开大学何良年教授课题组报道了一种芳基三氮烯与二氧化碳的电化学脱胺基羧基化反应,以构建结构多样的芳基羧酸衍生物(Scheme 1D)。参考文献:Org. Lett. 2025, 27, 4553–4558
文献信息:Electrochemical Deaminative Carboxylation of Aryltriazenes with CO2 to Aryl Carboxylic Acids
Lan Zhao, An-Guo Wu, Hong-Ru Li, Alexander O. Terent’ev, and Liang-Nian He*